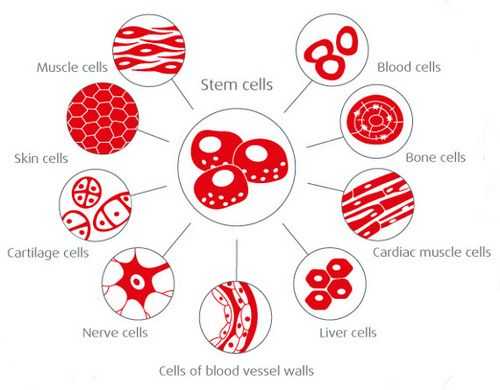
Regenerationsforskning i diabetes: Grundlæggende
Betaceller og holmer af Langerhans
Betacellerne er de insulinproducerende celler i bugspytkirtlen. De er ikke distribueret over vævet, men er samlet i specifikke regioner i organet – Langerhans holme, opkaldt efter deres opdager, Paul Langerhans.
Betaceller udgør 65 til 80 procent af Langerhans-holmene og omtales derfor undertiden som holme-celler. Neurotransmittere til stofskiftet. Alfaceller producerer hormonet glukagon, antagonisten mod insulin. Glucagon fremmer frigivelse af glukose fra leveren og får blodsukkerniveauet til at stige.
Den humane bugspytkirtel indeholder omkring en million holmer af Langerhans med ca. 4.000 beta-celler hver. Dog er det kun ca. 20 procent af betaceller, der er nødvendige for at producere tilstrækkeligt insulin til at regulere blodsukkerniveauet. Dette er grunden til, at type 1-diabetes først vises, når store dele af de insulinproducerende beta-celler allerede er blevet ødelagt af autoantistoffer..
Hvordan regulerer beta-cellemassen sig selv?
Det har været kendt i nogle få år, at beta-cellefunktion og beta-cellemasse i bugspytkirtlen er dynamisk reguleret. Med stigende kropsvægt eller under graviditet øges den funktionelt effektive beta-cellemasse. Cellerne forstørres, og nye beta-celler dannes. Gennem en dynamisk balance mellem vækst og celledød tilpasser beta-cellerne sig til de respektive metaboliske krav. Hvis denne balance er skæv, fører disse til en forstyrret glukosemetabolisme.
I både type 1-diabetes og avanceret type 2-diabetes falder den absolutte og funktionelle beta-cellemasse, når sygdommen skrider frem. Regenerering af beta-celler repræsenterer en lovende forskningsmetode. Dette kræver en forståelse af, hvordan betacellevækst reguleres. F.eks. Er glukagonlignende peptid 1 (GLP-1), vækstfaktorer (IGF-I og -II, PDGF, EGF), lactogener og glucose involveret.
Den tætte forbindelse mellem holmceller og blodkar spiller en vigtig rolle: Langerhans holme krydses af et tæt netværk af små blodkar (kapillærer). Hver beta-celle er i kontakt med mindst en blodkar-endotelcelle. Betacellen er direkte på blodsukkerniveauet og afhængigt af dette frigiver den passende mængde insulin i blodstrømmen.
Endotelcellerne regulerer opdelingen, funktionen og modningen af beta-cellerne og holder dem i et differentieret trin. Mus, der maler blodkar i deres Langerhans holme, kan blive diabetikere.
Molekylære afbrydere til celledifferentiering
Stien fra stamcelle til moden vævscelle er lang og styres af en række forskellige molekylære mekanismer. Forskere ved Helmholtz Zentrum München studerer intensivt dannelsen af beta-celler under embryonal udvikling. Cellsignaler, genregulatorer og molekyler, der regulerer morfogenese, er af stor interesse for at afkryptere sygdomsmekanismer.
Såkaldte pluripotente (fra latin ‘plus’, mere og ‘potens’, magtfulde, dygtige) stamceller har evnen til at udvikle sig til forskellige vævstyper. For at omdanne dem til beta-celler kræves omfattende viden om differentieringsmekanismer og tegninger.
Her finder du en video fra Vimeo. Med dit samtykke etableres en forbindelse til Vimeo. Vimeo bruger cookies alt efter hvad der er tilfældet. Klik her for mere information.
Regenerative terapier giver muligheder for helbredelse – for type 1 og også for type 2-diabetes. Professor Heiko Lickert, leder af Institut for diabetes og regenerationsforskning ved Helmholtz Zentrum München, forklarer de forskellige strategier i et videointerview. Længde: 2,33 minutter
Undersøgelse af betacellen i detaljer
Betacelleprogenitorerne er i stand til at udvikle sig til forskellige pancreascelletyper, såsom pancreaskanalceller eller forskellige typer kirtler. Når embryonal udvikling er afsluttet, bestemmes cellernes funktion, og cellerne mister evnen til at udvikle sig til andre celletyper.
Dette produkt er udviklet i meget lang tid. Hvis der dannes for få beta-celler på grund af defekter i embryonal udvikling, fødes personen med mindre beta-cellemasse og har en øget risiko for at udvikle diabetes. Forskerne har imidlertid mistanke om, at det multipliceres med opdeling. Denne division falder imidlertid kraftigt efter den tidlige barndoms udvikling og er næsten nul i en fyrre eller halvtreds år gammel person
Forskellige tilgange til regenerering af betaceller
Regenerationsforskning er ikke kun på udkig efter cellulære egenskaber, der kan bruges til at regulere vækst og opdeling, funktion og død af celler. Forskere er også på udkig efter detaljerede funktioner af insulinproducerende celler, der kan bruges til behandling af diabetes.
Følgende tilgange er tænkelige:
Stimulering af vækst og spredning af beta-celler. Hos ældre mennesker er dette imidlertid næsten umuligt.
Vendende tab af beta-cellefunktion: I både type 1 og type 2-diabetes er der tegn på, at beta-celler kan miste deres modenhedsstatus og regressere til et ikke-funktionelt forfaderstadium. Fra denne tilstand er det muligt, at cellerne gendannes og vender tilbage til deres funktion. Dette forklarer f.eks. Den hurtige succes med blodglukosekontrol efter bariatrisk kirurgi såsom ærmet gastrektomi (reduktion af mavestørrelsen). Selv efter mange år med type 1-diabetes findes der stadig funktionelle beta-celler i bugspytkirtlen. En lav egenproduktion af insulin kan være påviselig. Det er videnskabens opgave at bedre forstå processerne i cellerne for at stimulere cellerne til at fungere igen.
Dannelsen af beta-celler fra stamceller til andre væv (for eksempel bugspytkirtelkanalen) diskuteres derfor.
Konvertering af alfaceller til beta-celler: Dette vil imidlertid være vanskeligt at implementere i klinisk praksis.
Efter at have spist stiger glukoseniveauet i blodet og stimulerer frigørelsen af insulin. Der er en forstærkermekanisme til glukoseeffekten: Forskellige neurotransmittere optager receptorer på overfladen af beta-cellerne. Disse transmitterer signaler ind i celleindretningen og forbedrer optagelsen af glukose i beta-cellen.
Receptorer og insulin gåte
Frigivelsen af insulin fra beta-celler er underlagt en kompleks reguleringsmekanisme. På nuværende tidspunkt er ikke alle mekanismer kendt. Den vigtigste trigger til insulinudskillelse er det øgede glukoseniveau i blodet efter et måltid. Fin regulering formidles af et antal neurotransmittere. Thesis neurotransmitters dokker til visse receptorer på overfladen af beta-cellerne. Glukose bruger ikke disse receptorer.
Hvad der foregår her i detaljer?
Neurotransmitter-receptorerne blev inaktiveret. Det konstateres, at udskillelsen af insulin i disse dyr forstyrres på et tidligt tidspunkt, og at de udvikler diabetes mellitus. Hvordan sker det? Når beta-cellen modtager glukosesignalet, initieres insulinsekretion, og neurotransmitterne frigøres sammen med insulinet. Tese dokker derefter til receptorerne på celleoverfladen og forbedrer således optagelsen af glukose i beta-cellen. Det er et barn med forstærkningsmekanisme.
Men hvad sker der, hvis receptorerne for neurotransmitterne mangler eller signaleringskæden startes? Forstærkningsmekanismen er ikke aktiveret, hvilket betyder, at glukose ikke længere kan udløse sekretion af insulin. Derfor forbliver glukoseniveauet i blodet højt. Hvis det var muligt at bruge denne receptormedierede mekanisme specifikt, kunne insulinsekretion forbedres.
Aktuel forskning om emnet
Mere om dette emne
tæt
|
Related Posts
-

Perspektiver på regenerationsforskning i diabetes
Perspektiver på regenerationsforskning inden for diabetes Der er allerede en række lovende forskningsmetoder inden for regenerativ diabetesforskning, som…
-
Regenerationsforskning i diabetes: fremtidig anvendelse
Regenerationsforskning inden for diabetes: Fremtidige anvendelsesområder Terapier med stamceller Stamceller er håbet om moderne medicin. På den ene side…
-
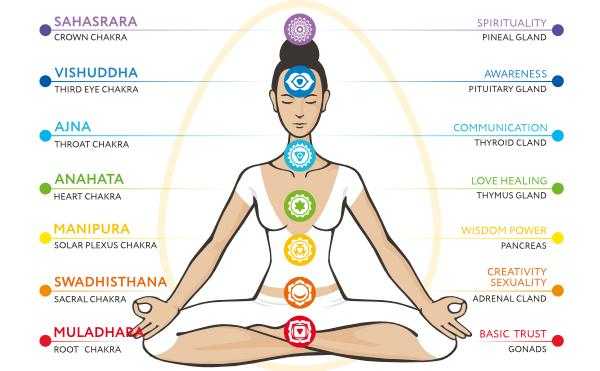
Ayurvedisk forfatningsbestemmelse, hotel bayernwinkel wellness-kurhotel
Ayurvedisk forfatningsbestemmelse Vata, Pitta eller / og Kapha; Hvem er jeg? Hvis du er interesseret i Ayurveda, vil du snart komme med spørgsmålet:…
-

Fødsel i hamburg: efter fødslen
Efter fødslen Hvis fødselen er ukompliceret, forbliver mor og barn på hospitalet i to til tre dage. I mange klinikker findes der nu en såkaldt 24-timers…
